はじめに
前のブログ記事(→滅菌と殺菌)で、滅菌、殺菌、消毒といった微生物やウイルスの制御について解説しました。そして記事の最後に感染症やパンデミックについての個人的考えを述べました。ここでは、感染症の拡大と抑制に関わる集団免疫 (herd immunity)について触れたいと思います。
病原微生物やウイルスによる感染症が世界的に拡大・流行すると、パンデミック(pandemic)と呼ばれます。記憶に新しいところでは、2009年の新型インフルエンザがあります [1]。またパンデミックではありませんが、2012–2013年に日本で風疹が流行しました [2]。近隣国では2002年-2003年に重症急性呼吸器症候群 (SARS) が中国を中心に発生し[3] 、2015年には韓国で中東呼吸器症候群(MERS)が流行りました [4, 5]。いずれもエンベロープ(後述)を有するRNAウイルスによる感染症です。
私たちの体は異物から身を守る自然免疫が備わっていますが、それとは別に病原微生物やウイルスによる病気にかかると獲得免疫ができます。すなわち、侵入してきた病原体の「形」を記憶し、次に同じ病原体が侵入してきたときにその抗体を発動してそれを無力化してしまいます。機構は異なりますが、獲得免疫システムは高等生物だけではなく、原核生物(アーキアおよびバクテリア) [6] にさえあることが最近わかってきました。
免疫を獲得することは感染症予防にとって重要なことです。この免疫が集団内でどのくらい広がるかが、感染症の拡大と抑制に重要な意味をもちます。これが集団免疫という概念です。
1. 集団免疫のメカニズム
集団免疫というのは、ある感染症に対して個人レベルではなく集団の大部分が免疫をもつことを指します。これは、感染症にかかった後の回復や予防接種を経ることで達成されますが、その結果として、その感染症に対する間接的な保護効果をもつようになります。すなわち、自然感染や予防接種による接触で集団内で多くの人が免疫をもつようになると、それらの免疫獲得者が防波堤となり、免疫を持たない人に対する保護効果が生まれるという理論です [7]。
集団免疫による感染症拡大抑制の概念を図1に示します。ある感染症にかかった一次感染者がいるとして、この感染者が次に何人に人に二次感染させるか(基本再生産数)が重要な数字であり、感染拡大のスピードを予測できるパラメータとなります。ここでは5人に二次感染させると考えます。集団免疫がないと病原体はすぐに5人の非免疫獲得者に感染するので、感染症は急速に拡大していきます(図1左)。一方で、80%の人に集団免疫があるとすると、感染は5人のうち1人にしか起こらず、急激な拡大は抑えられます(図1右、基本再生産数の減少)。
図1にみられるように、集団免疫の結果、
感染症はその連鎖が断ち切られて減衰するか拡大は緩やかなものとなります。当然ながら免疫獲得者の割合が高ければ高いほど、感染の拡大は抑えられることになります。集団内での
感染症拡大を止めるために必要な免疫獲得者の比率(臨海比率)を
集団免疫閾値と言います。
ここで、基本再生産数=
R0、集団免疫
閾値=
pとすると
p = 1 – (1/
R0)という関係式になります。たとえば基本再生産数が2であれば、集団免疫
閾値は0.5 (50%)となるわけです。2009年のインフルエンザ
パンデミックにおけるウイルスの場合、基本再生産数は2.3と報告されています
[8]。したがってこの場合は、理論上56%の人が免疫を獲得すれば集団内での病気伝染が抑制されることになります。
そして、実際の
感染症の流行において、
実効再生産数Rt = (1 –
p)
R0が1以下になれば、流行は収束する(減衰する)ということになります。
2. 予防接種の意義
集団免疫を人為的に拡大しようとするのが予防接種です。そして、子供への集団予防接種が
感染症の発生を抑え、非免疫獲得者に対する保護効果として現れた例として、日本における肺炎とインフルエンザによる死者数とワクチン接種との関係があります。2001年に発表された論文
[9] によれば、日本において集団ワクチン接種率(
灰色の棒グラフの部分)が高まると肺炎とインフルエンザによる高齢者の死者数(
折れ線グラフ)が減ったことが示されています(
図2)。
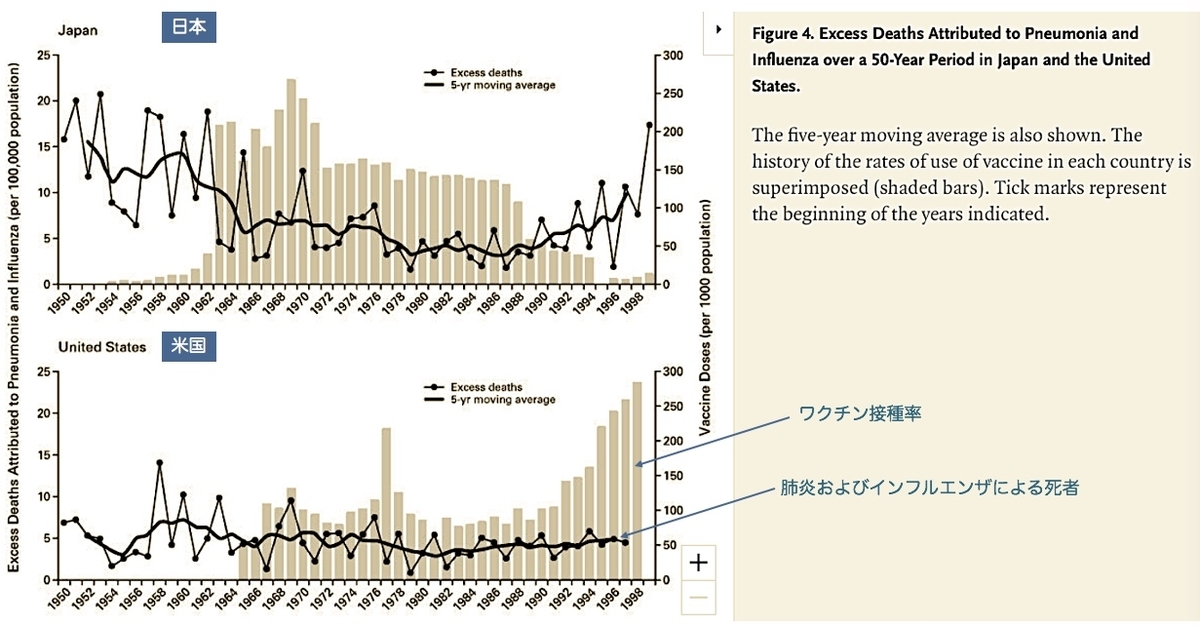
図2. 日本(上)および米国(下)における肺炎とインフルエンザの死者数とワクチン接種率との関係(文献 [9] からの転載図に加筆)
ただ、これはあくまでも現象論的な話なので、集団免疫の効果と同じようのものか、断定するのは難しいでしょう。
集団免疫の割合(全体で免疫をもつ人の割合)が一定のレベルに達すると、
感染症が集団から排除されるようになります。集団免疫による
感染症排除のメ
カニズムを使って撲滅されたのが
天然痘です。そのワクチンによる予防接種は
種痘と呼ばれ、日本では1976年まで続きました。それゆえそれまでに生まれた人は必ず種痘を受けているので、腕にその証拠としての瘢痕が残っています(
図3)。
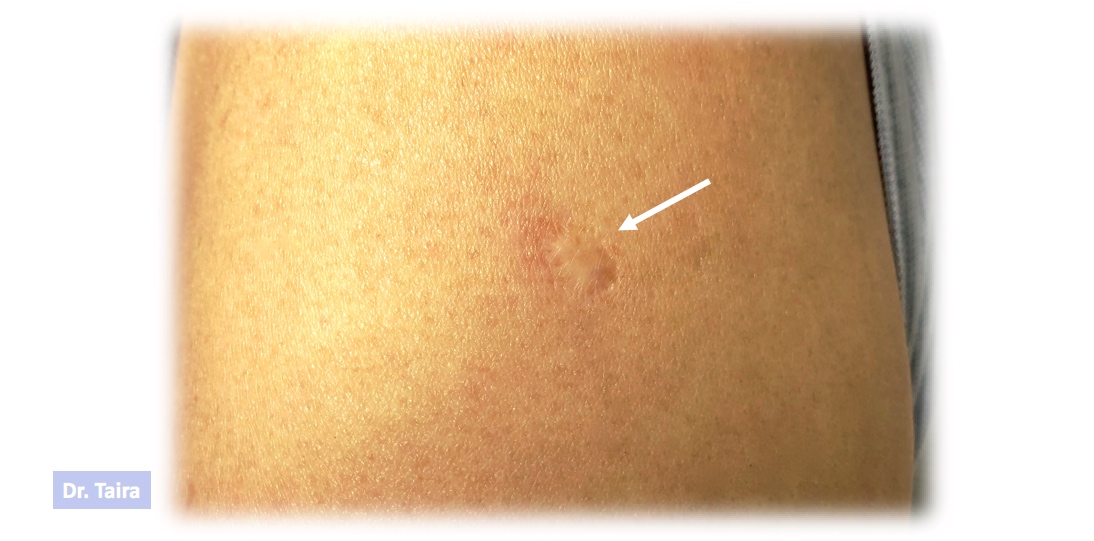
図3. 種痘による上腕の瘢痕(矢印)
天然痘は1980年に撲滅宣言されました。人類が初めて根絶に成功した
感染症です。その原因となる
天然痘ウイルスはもはや自然界には存在せず、米国とロシアの2施設にのみ保管されていると言われています。逆に言うと、もしこのウイルスが環境に漏出したら、あるいは
生物兵器として利用されたとしたら恐ろしいことになります。少なくとも1980年以降に生まれた人は
天然痘に対する免疫をもっていないのですから。
3. ウイルスの変異
ある
感染症に対する集団免疫が拡大すればその
感染症が永続的に抑制できるというものでもありません。なぜなら、ウイルスは集団免疫を回避するかのように
変異するからです
[10]。言い換えれば、
集団免疫が選択圧となってウイルスの変異を促すということです。免疫はウイルスの表面抗原(ウイルスの
カプシドや
エンベロープ上のタンパク質 [
図4])を認識して獲得されますが、この抗原をコードするウイルスの遺伝子に変異が起こると免疫は効かなくなります。このような変異を
抗原ドリフトといいます。
図5に
ウイルスの変異の様式を示します。変異には抗原ドリフトに加え、
抗原シフトがあります。抗原シフトとは同一種の異なるウイルス株の組み合わせによって生じる変異で、インフルエンザウイルスで起こりやすいことが知られています。
バクテリアからヒトまで生物のゲノムの複製は忠実に行われますが、ウイルスのそれは忠実度(fidelity)が低い(コピーミスを修復する機構がない)ために頻繁に変異が起こります。
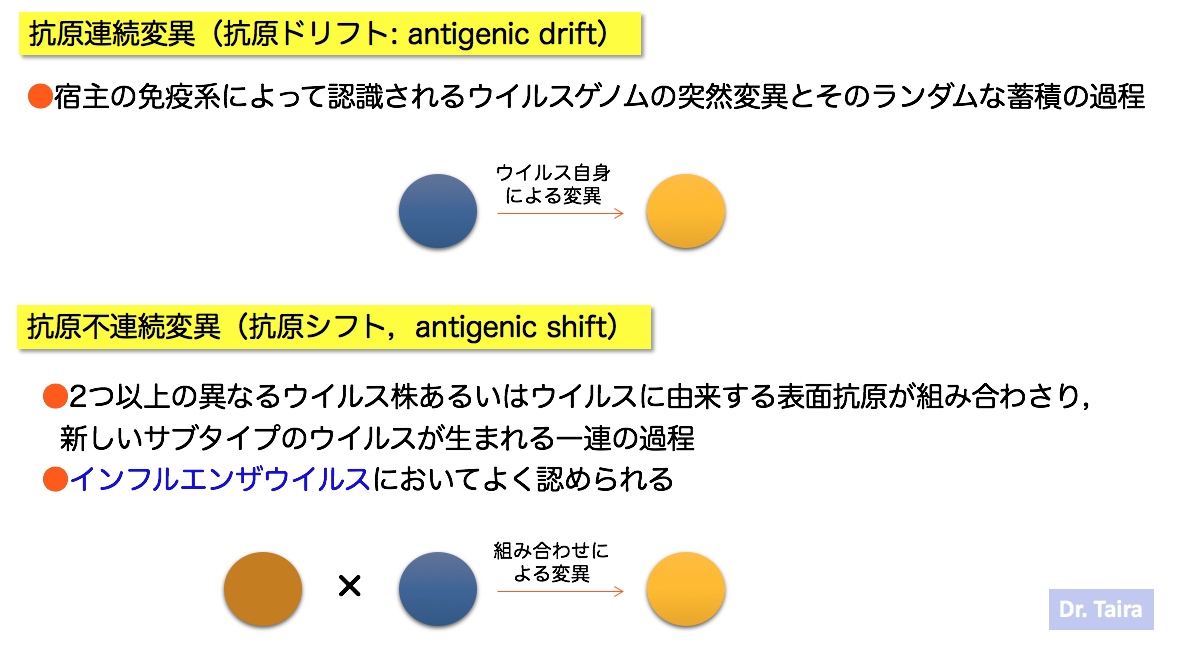
図5. ウイルスの変異の二つの様式:抗原ドリフトと抗原シフト
このような抗原ドリフトに類似したものに、
バクテリアにおける多剤耐性(大部分の
抗生物質が効かなくなること)を生じる変異があります。
抗生物質耐性は集団免疫のような生物学的な選択圧の結果ではありませんが、代わりに
抗生物質という化学物質が選択圧となって
バクテリアが多剤耐性プラスミドを獲得し、
抗生物質の攻撃をかわす仕組みです。ただし、
抗生物質耐性と免疫逃避(耐性)は根本的に異なるメ
カニズムで起こるので注意が必要です。
自然感染による集団免疫によって感染流行が沈静化したとする例は、私が知る限り明確に報告されていないように思います。その中でも、1918-
1920年に世界規模で流行した
スペイン風邪(インフルエンザ)は、記録にある限り人類が遭遇した最初の
パンデミックであり、5億人が感染したとされます
[11]。これでも当時の人口で約3割の感染者なので、集団免疫の理論に適合する終息と考えるには感染者数が小さすぎます。実際には、その収束(終息)においては、
自然免疫の機構もいっしょに働くのかもしれませんし、隔離という物理的要因なども影響しているのでしょう。
日本では、上記のインフルエンザで国民の4割弱が感染した(死者数38万人)とされていますので
[12]、局所的にはその沈静化に集団免疫のメ
カニズムが働いたかもしれません。基本(実効)再生産数=1.6という弱い感染力の場合、理論上成り立つ計算ですが、やはり隔離やその他の要因も加わっていると考えるのが妥当です。
上述したようにウイルスは抗原ドリフトによって集団免疫のバリアーから身をかわし、変異で新たな感染力を身につけます。さらに病原体が残る限り、世代を経れば集団免疫の効果もなくなり、新たな世代が感染の脅威に曝されます。2009年の
新型インフルエンザの流行はその例です。
天然痘のようにワクチン接種によって撲滅されない限り、
人類は常にパンデミックの可能性の下にいるのです。
パンデミックが起こった場合、それが
ワクチン接種による集団免疫効果で終息できるというのも不確定です。なぜなら、世界規模でのワクチン接種プログラムでは、地域や人種で接種率にムラを生じ、免疫力の時間的差異が生まれ、
非接種者の間で感染続く一方で、
ワクチン接種が拡大すれば、それに応じて免疫逃避のウイルス変異が起こる時間的余裕を与えるからです。
天然痘や麻疹のようにワクチンを打てば一生かからないという病気の場合と違って、
パンデミックを起こすようなウイルス病原体は、感染力が強く、致死率がそれなりに低く(たとえば<10%)、頻繁に変異を繰り返す機会があるという条件を備えていると考えられます。すなわち、上述したように、
パンデミック下でワクチン接種を行なうと抗原ドリフトを含む免疫逃避が起こり感染拡大する可能性もあるのです。
呼吸系ウイルスに対する抗体が時間経過とともに減衰することもよく知られている事実です。ワクチンが永続的に機能するウイルスとそうでないウイルスについて、それぞれ何がそうさせているのか詳細にはわかっていません。
人類はパンデミックを大量のワクチン接種で終息させた経験がまだありません。現時点においては、
集団免疫による保護効果はあくまでも理論上の話と捉えた方がよいです。
上述したように、集団免疫のメ
カニズムをうまく利用すれば、
感染症の集団への拡大を予測したり予防したりすることが理論的にはできます。私はまったくの門外漢ですが、
集団免疫の概念をベースにした数理モデルを活用して
感染症の拡大・流行は予測する研究が進められています
[13, 14, 15, 16]。すなわち、数式化された理論上の流行パターンを実際の流行の模倣としてコンピュータ上で再現するアプローチです
数理モデルの最も顕著な活用例の一つとしては、予防接種の設計が挙げられます。ある
感染症の集団免疫の広がり方について
数理モデルを構築できれば、これ以上の拡大を防ぐために、どの世代にワクチン接種をするのが効果的なのかを知ることができます。
一方で、従来の
数理モデルについてはいろいろと欠点も指摘されています。モデルの核となるパラメータは基本再生産数ですが、これまでのモデルは性別や年齢などにおける感染の様式の違い、感染者や非感染者の行動形態などは無視し、感染経路を単
純化しています
[16]。これらの欠点を克服するより効果的なモデルの研究が望まれます。
現在、
感染症に直接関わる病原体に関する科学的知見や
感染症例数などに関する膨大なデータベースに加えて、国境を越えた人の移動や物流のビックデータがストックされており、AIを駆使した
IT技術も日進月歩です。人の移動、感染ルートや様式などを加味した
数理モデルを活用はより正確な
感染症拡大の予測を可能とし、
感染症対策の設計に有効な示唆を与えると期待されます。
課題は、これから起こるであろう
新型感染症によるパンデミックへの対策です。感染力の強い新型ウイルスによる
感染症が発生し、危険ではあるがその平均致死率が低い場合(たとえば<10%)、
パンデミックに繋がる恐れがあります。その拡大と減衰の予測について、集団免疫の概念をベースとする手法はどの程度貢献できるのでしょうか。
よく専門家は、インフルエンザの例などに基づいて、「
6割以上の人が自然感染すれば集団免疫が広がり自然に抑制される」と言います。科学的一般論では、事実そうです。しかしそれでは身も蓋もありません。なぜなら、集団免疫で
感染症が抑制できたとしても、それには想像できないくらいの長期間を要するでしょうし、それまでの
健康被害、経済的損害、文化的被害を含めた社会的被害は甚大なものとなるからです。
仮に致死率1%の
感染症だとすると、日本では約7000万人以上が感染あるいは発症し、70万人以上の死者が出るということになります。実際には無症状感染や自然治癒の場合もあるので、確定患者当たりの致死率で1%で考えれば死者数はもっと低くなりますが、それでもそのような被害はとても許容できるものではありません。また、6割という感染率も、文献上過去に例はありません。
また「
できるだけ感染者数を低くしつつ、感染拡大のピークを遅らせて集団免疫が広がるのを待つ」という考え方もあります。これは新型
感染症への対処として、医療体制の維持(
医療崩壊の回避)・整備やワクチン開発までの時間稼ぎという面では意味はあるかもしれません。しかし、ウイルス学や疫学の観点からは上記の「6割以上の人が感染して集団免疫が拡大」という言い方を変えたに過ぎません。
実際に自然感染でどのくらい待てばいいのか予測はきわめてむずかしいと思われますし、現実的ではありません。社会が求めるのは、そのような予測
不能な中で、人的被害かつ経済的被害をできる限り少なくするという面からの具体的示唆です。
基本的に集団免疫が広がることと被害を少なくするということは相反します。集団免疫の獲得には多くの人が感染する必要があり、それが自然感染であれば
健康被害は甚大になります。このような集団免疫の考え方はすでにワクチンが開発され、予防接種が可能な場合に初めて有効となるものでしょう。実際には、ワクチンがあったとしても、上述したように、ウイルスの免疫逃避があるため、
パンデミック下においては
集団免疫の保護効果は一時しのぎという程度になるかもしれません。
新型病原体についてはもちろんワクチンはなく、その開発から
臨床試験→実用化→集団投与に至るまでには時間がかかります。その道へ突入すれば「ワクチン開発ーそれによる集団免疫の獲得」と「人的・経済的被害」を天秤にかける大きな賭けになります。
とはいえ、たとえばMERSや
SARSのような
コロナウイルスの場合は、ワクチン開発は具体化していません。やってみると技術的問題が出てきたとか、
感染症が地域的に限定されるなどの理由で、商業的に儲からないワクチンは開発されないのが常です。
人為的集団免疫拡大の戦略も資本主義の市場・経済原理と密接に結びついているのです。ただ、一般に
コロナウイルスの場合、抗体の効力は消失しやすいと言われていますし [
17]、実際にワクチンができたとしても、効力を長期間はたらかせるのはむずかしいとされています。
パンデミックでは甚大な被害が出ることが予想されますが、それをできる限り避けるという面からは集団免疫の意義を説いてもむしろ無意味でしょう。むしろ力技で封じ込める「
隔離」(
人の流れを断ち、接触をなくす)という方が現実的です。いずれにせよ、封じ込めは感染のピークを遅らせるという場合にも必要です。このような
接触削減の場合においても、国民の「
手洗い」や「(呼吸器系
感染症の場合)
マスク着用」をも含む徹底的な
公衆衛生学的管理が重要です(関連ブログ記事:
滅菌と殺菌)。
上記のような
隔離という手段の有効性については、集団免疫の理論が応用できます。上記のように、
実効再生産数Rt = (1 –
p)
R0 <1となればいいわけですから、同様に基本再生産数
R0 =2.3 とすると、
p = 0.56となります。つまり、>56%の人が集団免疫を獲得する代わりに、隔離(
接触削減)という物理的手段で感染者から遠ざかれば、全体として感染拡大は抑えられます。
実際に、人口の>56%を隔離するということは、ほとんど不可能です。もし、それに近い効果を期待するなら、緊急(非常)事態宣言とともに
都市封鎖(ロックダウン)という手段をとらなくてはいけません。日本では、2012年に施行された「
新型インフルエンザ等対策特別措置法」に緊急事態宣言の条項がありますが、都市封鎖という法的な強制力はありません。あくまでも要請のレベルでの人の遮断を実行するということになります。
また、
伝播の異質性 [
13] という人の属性の違いによって、感染形態は異なります。このように、要請レベルでの人の移動制限の達成率と伝播の異質性を考慮すれば、実際は、計算される
pの値よりも大きい割合の隔離(人の
接触遮断)が必要になってくると思われます。
さらに、
感染症流行とともに獲得免疫者が増えてきますので、その獲得免疫数と物理的な隔離数の総和が、感染拡大抑制に影響します。
感染症患者が数万人、数十万人規模になってくると、医療を圧迫し、そして医療機能不全の状態に陥ります。このようにして考えると、
健康被害と経済的被害を最小にするためには、
感染患者の爆発的増加によって医療崩壊が起きるかなり以前に、隔離という手段をとるのが、最もよいということになります。隔離は感染者と非感染者の両方に必要になりますので、検査・追跡調査によって感染の実態が正確に把握されていることが前提となります(
検査と隔離という感染拡大の予防原則)。
新型
感染症の拡大予測や抑制に対する
数理モデルの活用はどうでしょうか。この場合は、
感染症や病原体の情報(たとえば潜伏期はどのくらいか、一次感染者が何人に二次感染させるか、感染ルートなど)がほとんどないので、初動予測が立てにくくなるでしょう。リアルタイムでモデルを考えていくには、感染者の医療対応を進めながらの膨大な検査数と正確な感染者数の把握が必要ですので、そのときの国の方針・初動対策次第ということになります。少なくとも「隔離」という手段への集団免疫理論の応用については、
数理モデルが役に立つことは間違いないです。
おわりに
集団免疫の拡大と
感染症の沈静化の関係についてはすでに確立した理論です。一般的にはこの理論に基づく
感染症の拡大と衰退の予測は効率的ワクチン接種の設計などに貢献することが期待されます。インフルエンザの例でわかるように、若年層への予防接種増加によって高齢者の感染者の死亡数を減らす効果があることは、若年層の感染率と行動パターンが
感染症の拡大と抑制に影響を及ぼすこともわかります。
ただ、上述したように、
パンデミックが起こった場合、ワクチン接種による集団免疫効果がその終息に繋がるかということはわかりません。
人類はまだ経験したことがないのです。その意味で、将来の新型
感染症による
パンデミックに備えておくべきことはいろいろと見えてきます。情報不足の中では
健康被害や経済的被害を最小限にする拡大・沈静化予測は立てにくいものです。より効果的な
数理モデルの開発は無論のことですが、生物学的な集団免疫に頼らない方策(たとえば物理的隔離による対策)をもしっかりと考えておくべきです。
少なくとも想定できる対策は以下のとおりです。
感染症対策に関わる研究領域や保健所の人員を含めた予算措置、データベースの充実、検査体制(とくに
PCRなどの
核酸検査)の整備、
感染症に対応した医療提供体制の整備、ワクチンの開発・生産体制の拡大整備、学際的な専門家組織(微生物・ウイルス学、
感染症や医療の専門家はもちろん、
疫学、統計学、法学、社会学、経済学など)の構築とその情報を効果的に生かす政治・行政の体制の改善、公衆衛生で必要な消毒剤やマスクの備蓄などです。
引用文献・記事
[8] Biggerstaff, M. et al.: Estimates of the reproduction number for seasonal, pandemic, and zoonotic influenza: a systematic review of the literature
BMC Infect. Dis.
14: 480 (2014).
http://doi.10.1186/1471-2334-14-480.[10] Ramani, S. et al: Epidemiology of human noroviruses and updates on vaccine development. Curr. Opin. Gastroenterol.
30, 25–33 (2014). doi:
10.1097/MOG.0000000000000022.[14] 西浦博, 江島啓介.
感染症流行の
数理モデルを利用した予防接種の政策判断.最新医学
69, 786-794 (2014).
[15] 西浦博.
感染症流行の
数理モデルへの招待. 実験医学
33, 2798-2804 (2015).